„Killervirus“ SARS-CoV-2 und lösliches ACE2 (APN01) als Arzneimittel bei schwerer viraler Lungenkrankheit
Ein neuer Wirkstoff verhindert, dass das Corona-Virus (SARS-CoV-2) in die Zellen eindringt und gleichzeitig werden die Organe geschützt
Im Jahr 2003 erschreckte eine neue Erkrankung die Welt. Leute hatten Angst zu reisen, die Wirtschaft von Ländern und Städten wurde stark betroffen, und die Medien waren voll mit Schreckensmeldungen. Die Krankheit war SARS (severe acute respiratory syndrome). Sehr schnell war klar, dass ein neues Virus, das SARS- Coronavirus, für diese schwere Lungenerkrankung verantwortlich war.
Im Zuge der aktuellen globalen Krise durch das Corona Virus arbeiten Forscherteams weltweit an Strategien zur Eindämmung dieser Pandemie. Es ist ein Wettlauf gegen die Zeit. Um die Gesundheitssysteme der Welt vor dem Kollaps zu bewahren, braucht es rasch Medikamente, die vor allem bei schweren Verläufen zum Einsatz kommen können.
Ein lösliches Angiotensin Converting Enzyme 2 (rhACE2) oder auch als APN01 bezeichnet, ist ein von APEIRON entwickeltes biotechnologisch hergestelltes rekombinantes ACE2, das als Medikament eine duale Wirkungsweise hat:
Zum einen bindet sich das Virus an das lösliche ACE2 anstatt an das ACE2 an den Zellen. Das heißt, das Virus ist dann auf dem löslichen ACE2, dem APN01, und kann dadurch nicht die Zellen infizieren, sondern wird vom Immunsystem abgebaut.
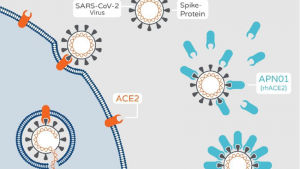
© Apeiron Biologics AG
Zum anderen kann es durch die Spaltung von Angiotensin-II in das unschädliche Angiotensin1-7 vor Lungenschäden schützen. Es kommt zur Reduzierung der schädlichen Entzündungsreaktionen in der Lunge und zum Schutz vor dem Lungenversagen, dem ARDS (Acute Respiratory Distress Syndrome).
Wie bei dem SARS-Virus ist auch bei SARS-Cov-2 das Protein ACE2 die Eintrittspforte für Viren, um Zellen in der Lunge zu infizieren. Gleichzeitig hat ACE2 eine zweite, wichtige Funktion als Blutdruckregulator.
SARS-CoV-2 ist mit dem damaligen SARS-Virus eng verwandt und es zeigte sich, dass dessen typischen „Spikes“, es sind Strukturen aus Proteinen an der Oberfläche des Virus, die zielgerichtet an die ACE2 Rezeptoren an Zell-Oberflächen andocken. Diese Andockstellen befinden sich nicht nur in der Lunge, sondern auch am Herzen, in den Blutgefäßen, im Darm und den Nieren, was die schweren Krankheitsverläufe von COVID-19 durch Organversagen und Sepsis erklären kann.
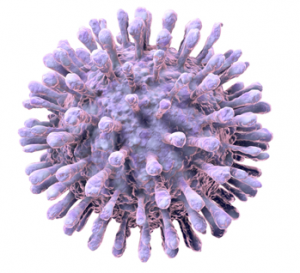
Abb. SARS-Coronavirus Spikes
Das Spike-Protein von SARS-CoV setzt sich aus zwei Untereinheiten zusammen. Die S1-Untereinheit enthält die rezeptorbindende Domäne (engl. receptor-binding domain, RBD), das an ACE2 binden kann. Bei Bindung der RBD an ACE2 verursacht dies Konformationsänderungen in der S2-Untereinheit, die eine Fusion der Virushülle mit der Zellmembran erleichtern.
Der ACE2-Rezeptor ist tatsächlich der Rezeptor, der das SARS-CoV-2 – Virus auffängt.
Somit nutzen SARS-Viren, als „Killervirus“, den ACE2-Rezeptor zum Eintritt in die Zellen, unter anderem in die Epithelzellen der Atemwege und die Parenchymzellen der Lunge und starten dann die Virusreplikation. Parallel dazu nimmt die ACE2-Expression in den Zellen ab und damit auch die Möglichkeit, Angiotensin II durch Umwandlung in Angiotensin1-7 zu entschärfen.
© IMBA/Kulscaz
Covid-19-Wirkstoff konnte erfolgreich bei Organoiden eingesetzt werden. Organoide sind winzige, organähnliche Strukturen, die man aus menschlichen Stammzellen kultivieren kann, um Krankheiten zu modellieren und Medikamente im menschlichen Zellverband zu testen. Blutgefäß-Organoide, sowie Nieren-Organoide wurden bereits 2018 am IMBA entwickelt. Es zeigte sich, dass das Virus die Organoide direkt infizieren und sich in diesen Geweben vervielfältigen kann. Die Gabe des Wirkstoffes APNO1 (hrACE2) reduzierte die SARS-CoV-2-Infektion in diesen künstlich hergestellten menschlichen Geweben. In Zellkulturen konnte die Viruslast durch hrACE2 (APNO1) um den Faktor 1.000-5.000 gemindert werden.
Literatur:
„Inhibition of SARS-CoV-2 infections in engineered human tissues using clinical-grade soluble human ACE2“, Monteil et al., Cell, 2020; DOI: 10.1016/j.cell.2020.04.004
Meilensteine des Forschungsteams von APEIRON mit P.M. Penninger:

Abb. JM Penninger
Apeiron Biologics AG, ein führendes Biotech-Unternehmen, das 2004 von Prof. Dr. Josef Martin Penninger gegründet und im IMBA – Institut für Molekulare Biotechnologie – in Wien domiziliert wurde.
2010 wurde das Unternehmen an das weltweit führende Pharma-Unternehmen GlaxoSmithKline (gsk) auslizensiert. Im Jahr 2019 erhielt APEIRON die APN01-Lizenzen von GlaxoSmithKline (gsk) für die weitere klinische Entwicklung zurück.
2012 erhielt IMBA- Gründungsdirektor Josef Martin Penninger den begehrten „Innovator Award“ für die Erforschung der Beteiligung des für den Knochenstoffwechsel wichtigen Proteins RANKL an der Brustkrebsentstehung.
Im Mai 2017 war die Zulassung des von Apeiron entwickelten monoklonalen Antikörpers APN311 (Dinutuximab beta, Qarziba®) für die Therapie von Patienten mit Neuroblastom-Erkrankung. Ein aktuelles klinische Programm mit APN401 von APEIRON entwickelt, ist eine autologe Zelltherapie zur Stärkung der Immunreaktivität über eine intra-zelluläre Master-Checkpoint (Cbl-b)-Blockade aus mit klein interferierender Ribonukleinsäure (siRNA) transfiziert stillgelegten peripheren mononukleären Blutzellen (PBMCs).
2020, APN01, ein von Apeiron entwickeltes biotechnologisch hergestelltes rekombinantes Angiotensin Converting Enzyme 2 (rhACE2) Arzneimittel, das die SARS-Cov-2 binden und vor akutem Lungenversagen schützen kann.
„Die von mir mitbegründete Biotechnologiefirma Apeiron setzt auf einen Wirkstoff, der verhindern soll, dass das Virus in die Zellen eindringt, gleichzeitig werden die Organe geschützt“ (J M Penninger).
Literatur:
Nicholls J, Peiris M, Nature Medicine 2005;11(8):821; Penninger JM et al. Nature Medicine 2005;11(8):875; Schneider MI, Molekulare Mechanismen des SARS.Coronavirus: Charakterisierung des Akzessorischen 7a-Proteins und Effekt des proteasomalen Inhibitors MG-132 auf die virale Replikation. Dissertation-Technische Universität-München. 2011
Der philosophische Begriff Apeiron, das „Unbegrenzte, Unermessliche“, als ein räumlich und zeitlich unbegrenzter Urstoff, wurde zuerst von Anaximander einem Schüler des Thales von Milet als » Prinzip alles Seienden« in die Philosophie eingeführt.
Für die Prävention empfehle ich grünen Tee und einen adäquaten Methylierungsstatus des Genoms.
Ihr Eduard Rappold
