
Oxidativer Stress und Alzheimer: Neue Erkenntnisse zu genetischen Einflussfaktoren und antioxidativer Abwehr
In einer aktuellen Studie, an der ich als Co-Autor mitwirken durfte (https://alz-journals.onlinelibrary.wiley.com/doi/10.1002/alz.70117), konnten wir neue Einblicke in die Rolle genetisch bedingter Veränderungen im antioxidativen System bei Alzheimer-Demenz (AD) gewinnen. Im Fokus standen dabei Enzyme wie Superoxiddismutase 1 (SOD1) und Glutathion-S-Transferase Omega 1 (GSTO1) – zentrale Akteure der zellulären Abwehr gegen oxidativen Stress.
Genetik trifft Biochemie: Das SNP rs4925 in GSTO1
Mittels genomischer Analysen identifizierten wir eine Variante im GSTO1-Gen (SNP rs4925), die mit erhöhten Enzymspiegeln in Blutplättchen assoziiert ist. Diese genetische Veränderung scheint eine kompensatorische Reaktion auf gesteigerten oxidativen Stress zu reflektieren – ein zentrales Merkmal bei Alzheimer. https://doi.org/10.1007/s00401-014-1341-8
SOD1 und CCS: Frühe Marker im Krankheitsverlauf
Neben GSTO1 war auch SOD1 signifikant erhöht – ein Enzym, das Superoxidradikale in Wasserstoffperoxid umwandelt. Auffällig war zudem, dass der Copper Chaperone for SOD1 (CCS) – essenziell für die Aktivierung von SOD1 – bereits im Frühstadium der kognitiven Beeinträchtigung (MCI) vermindert war. Dies könnte auf eine dysregulierte Aktivität trotz erhöhter SOD1-Level hindeuten.
Glutathionperoxidase 1 (GPX1) und Glutathion: Ein System in Schieflage
GPX1, das in enger Wechselwirkung mit SOD1 steht, war sowohl in Frontalhirnproben als auch in Blutplättchen reduziert. Diese Ergebnisse deuten auf eine gestörte Balance im Glutathion-System hin – einem der wichtigsten zellulären Schutzsysteme gegen oxidative Schäden.
SAM-e als möglicher therapeutischer Hebel
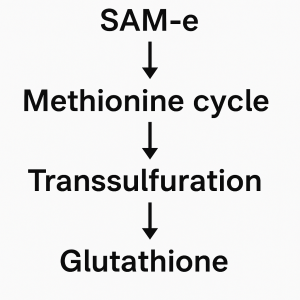
Ein vielversprechender therapeutischer Ansatz könnte die Modulation des Methionin-Zyklus sein – insbesondere über S-Adenosylmethionin (SAM-e). SAM-e ist nicht nur ein zentraler Methylgruppendonator für epigenetische Regulation, sondern auch Ausgangsstoff für die Transsulfurierung hin zum Glutathion-Stoffwechsel. Eine gezielte Unterstützung dieses Systems könnte die antioxidative Kapazität stärken und neuroprotektive Effekte entfalten.
Fazit
Unsere Ergebnisse unterstreichen die Bedeutung genetischer Varianten im oxidativen Stressnetzwerk bei Alzheimer und eröffnen neue Perspektiven für individualisierte Therapien. Die frühe Veränderung von SOD1 und CCS bereits im MCI-Stadium macht Hoffnung auf neue diagnostische Marker – und auf präventive Strategien, die gezielt in diese Netzwerke eingreifen, etwa über SAM-e.
Ihr
Eduard Rappold
Hinweis: Diese Informationen werden zu Bildungszwecken bereitgestellt und ersetzen keinen professionellen medizinischen Rat. Wenden Sie sich immer an Gesundheitsdienstleister, um eine individuelle Beratung zu gesundheitsbezogenen Fragen zu erhalten.
Copyright © Eduard Rappold 2025

SAM-e
mit (S/S)-Isomerpurity ist zu 100% bioaktiv
