
Spermidin – Schlüssel-Polyamin für Autophagie, Zellreinigung und gesunde Alterung
Biologische Bedeutung von Spermidin
Spermidin ist ein endogenes Polyamin, das in allen lebenden Zellen vorkommt, von Prokaryoten bis zum Menschen. Chemisch handelt es sich um ein kleines, positiv geladenes Molekül, das sich an DNA, RNA und Proteine binden kann und dadurch strukturelle und regulatorische Funktionen ausübt (Eisenberg et al., 2009; Madeo et al., 2018).
Spermidin ist ein Schlüsselfaktor der Zellhomöostase und spielt eine zentrale Rolle bei:
• Zellwachstum und Differenzierung
• epigenetischer Regulation
• Autophagie und Mitophagie
• Stabilisierung der Proteinsynthese
Seine besondere biologische Bedeutung liegt in seiner Funktion als Regulator zellulärer Erneuerungsprozesse.
Von SAM-e zu Spermidin: Der Polyamin-Stoffwechsel
Spermidin entsteht aus S-Adenosylmethionin (SAM-e) über den Polyamin-Stoffwechsel (Mato & Corrales, 2010):
- SAM-e wird zu decarboxyliertem SAM-e umgewandelt.
- Die dabei entstehenden Aminopropylgruppen werden auf Putrescin übertragen.
- Daraus entsteht Spermidin, anschließend Spermin.
Spermidin steht damit an einer Schnittstelle zwischen Methylierung, Redoxschutz und intrazellulärem Recycling.
Spermidin und Autophagie
Autophagie ist der zentrale Prozess für den Abbau und das Recycling geschädigter Zellbestandteile. Spermidin zählt zu den stärksten physiologischen Autophagie-Induktoren (Eisenberg et al., 2009; Morselli et al., 2011).
Zentrale Wirkmechanismen sind:
• Hemmung von EP300, einem Acetyltransferase-Enzym, das Autophagie normalerweise unterdrückt
• Aktivierung von AMPK- und SIRT1-abhängigen Signalwegen
• Erhöhte Expression autophagieassoziierter Gene (ATG7, LC3, Beclin-1)
Die funktionellen Folgen sind:
• Entfernung fehlgefalteter Proteine
• selektiver Abbau geschädigter Mitochondrien (Mitophagie)
• Stabilisierung der zellulären Energieproduktion
• Verlängerung der funktionellen Zelllebensdauer
Epigenetische und molekulare Wirkungen
Spermidin beeinflusst die Chromatinstruktur durch elektrostatische Bindung an die negativ geladene DNA. Dadurch verändert sich die räumliche Organisation der Nukleosomen und damit die Zugänglichkeit für Transkriptionsfaktoren (Madeo et al., 2018).
Zusätzlich moduliert Spermidin direkt die epigenetische Enzymausstattung:
• Aktivierung von Histon-Acetyltransferasen (HATs)
• Hemmung ausgewählter Histon-Deacetylasen (HDACs)
• Förderung transkriptionsbereiter Chromatinzustände
Auf Zellebene führt dies zu:
• erhöhter Stressresilienz
• stabilisierter mRNA- und rRNA-Struktur
• effizienterer Proteinsynthese
• Aktivierung der Autophagie und Mitophagie
Spermidin wirkt damit als zentraler Regulator des Gleichgewichts zwischen Genexpression, Proteostase und Organellenerneuerung.
Langlebigkeit und Gesundheitsspanne
In zahlreichen Modellorganismen verlängert Spermidin die Lebensspanne (Eisenberg et al., 2009; Morselli et al., 2011). Beim Menschen zeigen epidemiologische Studien Zusammenhänge zwischen hoher Spermidinaufnahme und:
• reduziertem kardiovaskulären Risiko
• geringerer Gesamtmortalität
• besserer Erhaltung kognitiver Funktionen im Alter (Kiechl et al., 2018)
Diese Effekte beruhen auf der gleichzeitigen Stabilisierung von Autophagie, mitochondrialer Funktion, Entzündungsregulation und epigenetischer Steuerung.
Quellen, endogene Spiegel und Ernährung
Spermidin ist natürlicherweise in vielen Lebensmitteln enthalten, insbesondere in:
• Weizenkeimen
• Sojabohnen
• Hülsenfrüchten
• Pilzen
• gereiftem Käse
• grünem Gemüse
Mit zunehmendem Alter sinken die endogenen Spermidinspiegel parallel zur Abnahme von SAM-e-Verfügbarkeit, mitochondrialer Aktivität und Autophagieeffizienz (Madeo et al., 2018). Eine spermidinreiche Ernährung oder standardisierte Extrakte können diese Abnahme teilweise kompensieren.
Spermidin in Pflanzen und Bakterien – eine evolutionär konservierte Regenerationsachse
Spermidin ist kein exklusiv menschliches Molekül, sondern ein evolutionär hochkonserviertes Polyamin, das in Pflanzen und Bakterien grundlegende Ordnungs- und Erneuerungsfunktionen erfüllt. Seine biologische Bedeutung liegt in der Stabilisierung von Wachstum, Stressresistenz und zellulärer Selbstorganisation – lange bevor komplexe Gewebe oder Nervensysteme existierten.
In Pflanzen reguliert Spermidin:
- Zellteilung, Differenzierung und Gewebeentwicklung,
- Stressantworten auf Trockenheit, Salz, Hitze und oxidative Belastung,
- Autophagie-ähnliche Recyclingprozesse und Verzögerung der Seneszenz.
Spermidin stabilisiert dabei DNA- und Membranstrukturen und unterstützt die Wiederherstellung metabolischer Ordnung unter Umweltstress. Besonders hohe Gehalte finden sich in keimenden Samen, Hülsenfrüchten, Weizenkeimen, Sojabohnen und grünem Blattgemüse.
In Bakterien, einschließlich vieler Darmmikroorganismen, ist Spermidin essenziell für:
- Stabilisierung von DNA und RNA,
- Wachstum, Zellteilung und Biofilm-Organisation,
- Widerstandsfähigkeit gegenüber pH-, Redox- und Osmoseschwankungen.
Viele Darmbakterien synthetisieren Spermidin selbst oder nehmen es aus der Nahrung auf und geben es teilweise an den Wirt weiter.
Gemeinsam bilden Pflanzen, Bakterien und menschliche Zellen eine kontinuierliche Spermidin-Achse, in der dasselbe Molekül:
- in Pflanzen Anpassung ermöglicht,
- im Mikrobiom ökologische Stabilität sichert,
- im Menschen Autophagie, epigenetische Ordnung und mitochondriale Qualitätssicherung fördert.
Spermidin steht damit exemplarisch für ein Prinzip biologischer Gesundheit:
Regeneration ist kein isolierter Prozess einzelner Organismen, sondern ein geteiltes, evolutionär abgestimmtes Programm.
Klinische Bedeutung und Prävention
Spermidin gilt als epigenetisch wirksames Nutraceutical, da es:
• Genregulation moduliert
• Autophagie aktiviert
• mitochondriale Funktion stabilisiert
• entzündliche Signalwege dämpft
Günstige Effekte wurden beschrieben bei:
• Herz-Kreislauf-Erkrankungen (Kiechl et al., 2018)
• Neurodegeneration (Eisenberg et al., 2009; Madeo et al., 2018)
• Lebererkrankungen (Morselli et al., 2011; Pietrocola et al., 2016)
Die Wirkung beruht auf systemischer zellulärer Reorganisation, nicht auf einer pharmakologischen Einzelwirkung.
Infobox: Spermidin als Autophagie-Schalter
Spermidin ist einer der stärksten bekannten endogenen Induktoren der Autophagie. Es wirkt nicht als klassisches Antioxidans oder Hormon, sondern als epigenetisch-metabolischer Schalter, der zelluläre Aufräum- und Erneuerungsprogramme aktiviert.
Zentrale Wirkmechanismen:
- Hemmung von EP300 (p300):
Spermidin inhibiert die Acetyltransferase EP300, ein Enzym, das Autophagie normalerweise unterdrückt. Die EP300-Hemmung verschiebt das zelluläre Programm von Wachstum zu Recycling. - Aktivierung autophagieassoziierter Gene:
Erhöhte Expression von ATG-Genen (z. B. ATG7, LC3, Beclin-1) fördert den Abbau fehlgefalteter Proteine und geschädigter Organellen. - Förderung von Mitophagie:
Selektive Entfernung dysfunktionaler Mitochondrien senkt ROS-Last und stabilisiert die mitochondriale Energieproduktion. - Kopplung an AMPK- und SIRT1-Signalwege:
Spermidin unterstützt energie- und redoxabhängige Reparaturprogramme und verbessert die Rückkehr in einen regulativen Grundzustand.
Biologische Konsequenzen:
- verbesserte Proteostase
- erhöhte Stressresilienz
- reduzierte Entzündungsaktivität
- verlangsamte epigenetische Alterung
Einordnung:
Spermidin schaltet Autophagie nicht als Notfallreaktion ein, sondern als strategisches Erneuerungsprogramm. Es ermöglicht der Zelle, Belastung nicht nur zu überstehen, sondern strukturell daraus zu lernen. Autophagie erscheint damit nicht als Abbauprozess, sondern als Voraussetzung nachhaltiger biologischer Ordnung.
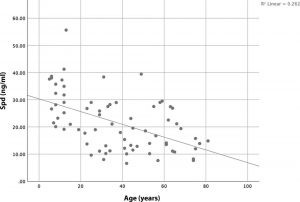
Abbildung 19 — Zusammenhang zwischen Alter und Spermidin-Konzentration im Plasma
Streudiagramm mit linearer Regressionslinie zur Darstellung der Beziehung zwischen Lebensalter (Jahre) und Spermidin-Konzentration (Spd, ng/ml). Zwischen Alter und Serum-Spermidin besteht ein signifikanter negativer Zusammenhang (r = −0,512; p < 0,001). Mit zunehmendem Lebensalter sinken die Spermidinspiegel deutlich, was auf eine altersabhängige Einschränkung polyaminvermittelter Regulationsmechanismen hinweist.
Quelle: Eigene grafische Darstellung nach Pekar et al., basierend auf publizierten Daten; keine originalgetreue Reproduktion.
Einordnung
Spermidin ist ein zentrales endogenes Polyamin und ein Schlüsselregulator zellulärer Erneuerung. Es entsteht aus S-Adenosylmethionin (SAM-e) im Polyamin-Stoffwechsel und verbindet damit Methylierungsökonomie, Redoxschutz und intrazelluläres Recycling zu einem funktionellen Kontinuum (Mato & Corrales, 2010; Madeo et al., 2018).
Auf molekularer Ebene stabilisiert Spermidin Chromatinstrukturen, moduliert epigenetische Enzyme und fördert transkriptionsbereite Zustände. Seine zentrale biologische Wirkung liegt in der Aktivierung der Autophagie durch EP300-Hemmung sowie AMPK- und SIRT1-abhängige Programme (Eisenberg et al., 2009).
Diese Prozesse verbessern Proteostase, mitochondriale Qualitätssicherung und Stressresilienz. In Modellorganismen verlängert Spermidin die Lebensspanne; beim Menschen ist eine höhere Aufnahme mit geringerer Mortalität und erhöhter Gesundheitsspanne assoziiert (Kiechl et al., 2018).
Spermidin wirkt nicht isoliert pharmakologisch, sondern als systemischer Regulator zellulärer Qualitätssicherung. Es steht exemplarisch für epigenetisch vermittelte Regeneration: Gesundheit beruht nicht auf Stillstand, sondern auf kontinuierlicher Erneuerung biologischer Ordnung.
Eduard Rappold
Note: This information is provided for educational purposes only and does not replace professional medical advice. Always consult qualified healthcare professionals for medical concerns.
Copyright © Eduard Rappold 2026
http://nugenis.eu/shop
NUGENIS specializes in epigenetically active nutritional supplements


